লেখক:
Judy Howell
সৃষ্টির তারিখ:
27 জুলাই 2021
আপডেটের তারিখ:
23 জুন 2024

কন্টেন্ট
- পদক্ষেপ
- অংশ 1 এর 1: কাঠামো বোঝা
- 4 অংশের 2: প্রতীক এবং নাম বোঝা
- 4 অংশ 3: পরমাণু সংখ্যা পড়া
- 4 এর 4 র্থ অংশ: পারমাণবিক ভর পড়া
উপাদানগুলির পর্যায় সারণি এ পর্যন্ত পাওয়া 118 টি উপাদানের একটি তালিকা। বেশ কয়েকটি চিহ্ন এবং সংখ্যা রয়েছে যা উপাদানগুলির মধ্যে পার্থক্য নির্দেশ করে, যখন টেবিলের কাঠামোটি মিলগুলি অনুসারে উপাদানগুলিকে সংগঠিত করে। আপনি নীচের নির্দেশিকাগুলি ব্যবহার করে পর্যায় সারণি পড়তে পারেন।
পদক্ষেপ
অংশ 1 এর 1: কাঠামো বোঝা
 পর্যায় সারণিটি ভাবুন যেন এটি শীর্ষ বাম দিকে শুরু হয় এবং শেষ সারি, নীচে এবং ডানদিকে শেষ হয়। টেবিলটি বর্ধমান পারমাণবিক সংখ্যার ক্রমে বাম থেকে ডানে কাঠামোযুক্ত। পারমাণবিক সংখ্যা হ'ল একক পরমাণুতে প্রোটনের সংখ্যা।
পর্যায় সারণিটি ভাবুন যেন এটি শীর্ষ বাম দিকে শুরু হয় এবং শেষ সারি, নীচে এবং ডানদিকে শেষ হয়। টেবিলটি বর্ধমান পারমাণবিক সংখ্যার ক্রমে বাম থেকে ডানে কাঠামোযুক্ত। পারমাণবিক সংখ্যা হ'ল একক পরমাণুতে প্রোটনের সংখ্যা। - প্রতিটি সারি বা কলাম সম্পূর্ণ নয়। কেন্দ্রে ফাঁক থাকতে পারে, বাম থেকে ডানে টেবিলটি পড়তে থাকুন। উদাহরণস্বরূপ, হাইড্রোজেনের পারমাণবিক সংখ্যা 1 এবং এটি শীর্ষ বাম কোণে অবস্থিত। হিলিয়ামের পারমাণবিক সংখ্যা 2 এবং এটি শীর্ষে ডানদিকে রয়েছে।
- 57 57 থেকে 71১ পর্যন্ত উপাদানগুলিকে সাধারণত টেবিলের নীচের ডানদিকে একটি উপসেট হিসাবে চিত্রিত করা হয়। এগুলি হল "বিরল পৃথিবী উপাদান"।
 সারণীর প্রতিটি কলামে আপনি উপাদানগুলির একটি "গ্রুপ" পাবেন। 18 টি কলাম রয়েছে।
সারণীর প্রতিটি কলামে আপনি উপাদানগুলির একটি "গ্রুপ" পাবেন। 18 টি কলাম রয়েছে। - উপরে থেকে নীচে পড়তে "একটি দলকে পড়া" শব্দটি ব্যবহার করুন।
- নম্বরগুলি সাধারণত কলামগুলির উপরে নির্দেশিত হয়; তবে এটি অন্যান্য গোষ্ঠীর অধীনেও হতে পারে যেমন ধাতু।
- পর্যায় সারণীতে ব্যবহৃত সংখ্যাটি প্রচুর পরিমাণে পৃথক হয়। এগুলি রোমান (আইএ), আরবি (1 এ) বা 1 থেকে 18 নম্বর হতে পারে।
- হাইড্রোজেন হ্যালোজেন পরিবার এবং ক্ষারীয় ধাতু বা উভয় ক্ষেত্রে থাকতে পারে।
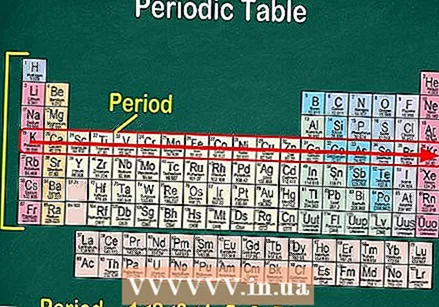 সারণির প্রতিটি সারিতে আপনি উপাদানগুলির "পিরিয়ডস" পাবেন। 7 পিরিয়ড রয়েছে। বাম থেকে ডানে পড়ার জন্য "একটি পিরিয়ড বরাবর পড়ুন" বাক্যাংশটি ব্যবহার করুন।
সারণির প্রতিটি সারিতে আপনি উপাদানগুলির "পিরিয়ডস" পাবেন। 7 পিরিয়ড রয়েছে। বাম থেকে ডানে পড়ার জন্য "একটি পিরিয়ড বরাবর পড়ুন" বাক্যাংশটি ব্যবহার করুন। - পিরিয়ডগুলি সাধারণত টেবিলের বাম দিকে 1 থেকে 7 নম্বরযুক্ত হয়।
- প্রতিটি পিরিয়ড শেষের চেয়ে বেশি। এটি পর্যায় সারণীতে পরমাণুর শক্তির স্তর বৃদ্ধির সাথে সম্পর্কিত।
 ধাতব, আধা-ধাতব এবং নন-ধাতব অতিরিক্ত গ্রুপগুলি বুঝতে। রঙগুলি ব্যাপকভাবে পরিবর্তিত হয়।
ধাতব, আধা-ধাতব এবং নন-ধাতব অতিরিক্ত গ্রুপগুলি বুঝতে। রঙগুলি ব্যাপকভাবে পরিবর্তিত হয়। - গ্রুপ ধাতুগুলির একটি রঙ রয়েছে। তবে হাইড্রোজেনের প্রায়শই নন-ধাতবগুলির মতো রঙ এবং গ্রুপ থাকে has ধাতুগুলির দীপ্তি থাকে, সাধারণত ঘরের তাপমাত্রায় শক্ত থাকে, তাপ এবং বিদ্যুত পরিচালনা করে এবং ম্যালেবল এবং ম্যালেবল হয়।
- নন-ধাতবগুলির একই রঙ রয়েছে। এগুলি হ'ল এইচ -1 (হাইড্রোজেন) সহ আরএন-C through এর মাধ্যমে সি-6 উপাদান। তাদের কোনও গ্লস নেই, তাপ এবং বিদ্যুত পরিচালনা করে এবং ম্যালেবল নয়। এগুলি সাধারণত ঘরের তাপমাত্রায় একটি গ্যাস তৈরি করে এবং এটি একটি কঠিন, গ্যাস বা তরল হতে পারে।
- অন্যান্য দুটি রঙের সংমিশ্রণ হিসাবে আধা-ধাতব / ধাতব প্রান্তগুলিতে সাধারণত বেগুনি বা সবুজ রঙ থাকে। লাইনটি তির্যক, বি -5 থেকে শুরু করে 85-পর্যন্ত অবধি বিস্তৃত। তাদের ধাতব এবং কিছু ধাতবগুলির কিছু বৈশিষ্ট্য রয়েছে।
 নোট করুন যে উপাদানগুলি মাঝে মধ্যে পরিবারে তালিকাভুক্ত হয়। এগুলি হ'ল ক্ষারীয় ধাতু (1 এ), ক্ষারীয় ধাতু (2 এ), হ্যালোজেনস (7 এ), আভিজাতীয় গ্যাস (8 এ) এবং কার্বন পরমাণু (4 এ)।
নোট করুন যে উপাদানগুলি মাঝে মধ্যে পরিবারে তালিকাভুক্ত হয়। এগুলি হ'ল ক্ষারীয় ধাতু (1 এ), ক্ষারীয় ধাতু (2 এ), হ্যালোজেনস (7 এ), আভিজাতীয় গ্যাস (8 এ) এবং কার্বন পরমাণু (4 এ)। - নম্বরটি রোমান, আরবি বা স্ট্যান্ডার্ড নম্বর হতে পারে।
4 অংশের 2: প্রতীক এবং নাম বোঝা
 প্রথমে প্রতীকটি পড়ুন। এটি এক বা দুটি বর্ণ নিয়ে গঠিত এবং বেশ কয়েকটি ভাষায় স্ট্যান্ডার্ড।
প্রথমে প্রতীকটি পড়ুন। এটি এক বা দুটি বর্ণ নিয়ে গঠিত এবং বেশ কয়েকটি ভাষায় স্ট্যান্ডার্ড। - প্রতীকটি উপাদানটির লাতিন নাম বা এর সাধারণ প্রচলিত বর্ণ থেকে নেওয়া যেতে পারে।
- অনেক ক্ষেত্রে, প্রতীকটি ইংলিশ নামকরণ কনভেনশন অনুসরণ করে, যেমন হিলিয়াম বা "তিনি"। যাইহোক, এটি এমন কোনও নিয়ম নয় যা আপনি ধরে নিতে পারেন। আয়রন, উদাহরণস্বরূপ, "ফে"। এই কারণে, দ্রুত উল্লেখের জন্য প্রতীক / নামের সংমিশ্রণটি সাধারণত মনে রাখা হয়।
 সাধারণ নাম তাকান। এটি সরাসরি প্রতীকের নীচে। পর্যায় সারণিটি যে ভাষায় লেখা হয় তার উপর নির্ভর করে এটি পৃথক হয়।
সাধারণ নাম তাকান। এটি সরাসরি প্রতীকের নীচে। পর্যায় সারণিটি যে ভাষায় লেখা হয় তার উপর নির্ভর করে এটি পৃথক হয়।
4 অংশ 3: পরমাণু সংখ্যা পড়া
 প্রতিটি উপাদানটির বাক্সের শীর্ষ কেন্দ্রে পারমাণবিক সংখ্যা অনুযায়ী পর্যায় সারণি পড়ুন। পূর্বে উল্লিখিত হিসাবে, সিস্টেমটি উপরের বাম থেকে নীচে ডানদিকে অর্ডার করা হয়। পারমাণবিক সংখ্যা জানার উপাদান সম্পর্কে আরও তথ্য সন্ধান করার দ্রুততম উপায় way
প্রতিটি উপাদানটির বাক্সের শীর্ষ কেন্দ্রে পারমাণবিক সংখ্যা অনুযায়ী পর্যায় সারণি পড়ুন। পূর্বে উল্লিখিত হিসাবে, সিস্টেমটি উপরের বাম থেকে নীচে ডানদিকে অর্ডার করা হয়। পারমাণবিক সংখ্যা জানার উপাদান সম্পর্কে আরও তথ্য সন্ধান করার দ্রুততম উপায় way 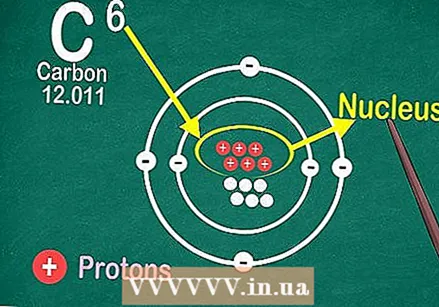 পারমাণবিক সংখ্যা হ'ল উপাদানটির একক পরমাণুর নিউক্লিয়াসে প্রোটনের সংখ্যা।
পারমাণবিক সংখ্যা হ'ল উপাদানটির একক পরমাণুর নিউক্লিয়াসে প্রোটনের সংখ্যা। প্রোটন যুক্ত বা অপসারণ একটি পৃথক উপাদান তৈরি করে।
প্রোটন যুক্ত বা অপসারণ একটি পৃথক উপাদান তৈরি করে। একটি পরমাণুতে প্রোটনের সংখ্যা অনুসন্ধান করাও ইলেক্ট্রনের সংখ্যা নির্ধারণ করে। পরমাণুতে প্রোটনের মতো ইলেকট্রন রয়েছে।
একটি পরমাণুতে প্রোটনের সংখ্যা অনুসন্ধান করাও ইলেক্ট্রনের সংখ্যা নির্ধারণ করে। পরমাণুতে প্রোটনের মতো ইলেকট্রন রয়েছে। - মনে রাখবেন যে এই নিয়মের ব্যতিক্রম আছে। যখন পরমাণু ইলেকট্রন হারাতে বা লাভ করে তখন এটি বৈদ্যুতিক চার্জ আয়ন হয়ে যায়।
- যদি উপাদানটির চিহ্নের পাশে একটি প্লাস চিহ্ন থাকে তবে এটি ইঙ্গিত দেয় যে এটি ইতিবাচকভাবে চার্জযুক্ত। বিয়োগ চিহ্ন সহ, এটি নেতিবাচকভাবে চার্জ করা হয়।
- যদি কোনও প্লাস বা বিয়োগ চিহ্ন না থাকে এবং আপনার রসায়ন সমস্যা আয়নগুলির বিষয়ে না হয় তবে প্রোটন এবং ইলেকট্রনের সংখ্যা সম্ভবত সমান।
4 এর 4 র্থ অংশ: পারমাণবিক ভর পড়া
 পারমাণবিক ভর নির্ধারণ করুন। এটি উপাদানটির সাধারণ নামের নীচের সংখ্যা।
পারমাণবিক ভর নির্ধারণ করুন। এটি উপাদানটির সাধারণ নামের নীচের সংখ্যা। - যদিও এটি দেখে মনে হতে পারে যে পারমাণবিক ভর সিস্টেমের উপরের বাম থেকে নীচে ডান দিকে বৃদ্ধি পাচ্ছে, এটি সব ক্ষেত্রেই সত্য নয়।
 বুঝতে পারেন যে বেশিরভাগ উপাদান দশমিক স্থান দ্বারা প্রতিনিধিত্ব করা হয়। পারমাণবিক ভর নিউক্লিয়াসের মোট কণাগুলি; তবে এটি বিভিন্ন আইসোটোপের ওজনযুক্ত গড়।
বুঝতে পারেন যে বেশিরভাগ উপাদান দশমিক স্থান দ্বারা প্রতিনিধিত্ব করা হয়। পারমাণবিক ভর নিউক্লিয়াসের মোট কণাগুলি; তবে এটি বিভিন্ন আইসোটোপের ওজনযুক্ত গড়।  একক পরমাণুতে নিউট্রনের সংখ্যা খুঁজতে পারমাণবিক ভর ব্যবহার করুন। পারমাণবিক ভরকে নিকটতম পূর্ণসংখ্যা, ভর সংখ্যাকে গোল করে। তারপরে নিউট্রনের সংখ্যা নির্ধারণ করতে আপনি ভর সংখ্যা থেকে প্রোটনের সংখ্যা বিয়োগ করুন।
একক পরমাণুতে নিউট্রনের সংখ্যা খুঁজতে পারমাণবিক ভর ব্যবহার করুন। পারমাণবিক ভরকে নিকটতম পূর্ণসংখ্যা, ভর সংখ্যাকে গোল করে। তারপরে নিউট্রনের সংখ্যা নির্ধারণ করতে আপনি ভর সংখ্যা থেকে প্রোটনের সংখ্যা বিয়োগ করুন। - উদাহরণস্বরূপ: লোহার পারমাণবিক ভর 55.847, সুতরাং এর ভর সংখ্যা 56 56 উপাদানটিতে 26 টি প্রোটন রয়েছে। ৫ ((ভর সংখ্যা) বিয়োগ ২ 26 (প্রোটন) হ'ল 30. একক লোহার পরমাণুতে সাধারণত 30 টি নিউট্রন থাকে।
- পরমাণুর নিউট্রনের সংখ্যা পরিবর্তন করে আইসোটোপ তৈরি হয় যা পরমাণুর ভারী বা হালকা সংস্করণ।