লেখক:
Randy Alexander
সৃষ্টির তারিখ:
2 এপ্রিল 2021
আপডেটের তারিখ:
1 জুলাই 2024
কন্টেন্ট
রাসায়নিক সমীকরণ একটি রাসায়নিক বিক্রিয়াটির প্রতীকী উপস্থাপনা। রিজেন্টগুলি বাম-হাতের এবং ডানদিকে পণ্য লেখা হয়। ভর সংরক্ষণের আইনটি ইঙ্গিত দেয় যে কোনও রাসায়নিক পদার্থে কোনও পরমাণু জন্মগ্রহণ বা হারিয়ে যায় না, তাই বিক্রিয়াটিতে উপস্থিত পরমাণুর সংখ্যা অবশ্যই বিক্রিয়ায় উপস্থিত পরমাণুর সংখ্যার সমান হতে হবে। পণ্য। এই টিউটোরিয়ালটি অনুসরণ করে আপনি রাসায়নিক সমীকরণকে বিভিন্ন উপায়ে ভারসাম্য বজায় রাখতে পারেন।
পদক্ষেপ
পদ্ধতি 1 এর 1: প্রচলিত পদ্ধতি অনুসারে ভারসাম্য
প্রদত্ত সমীকরণটি লিখুন। এই উদাহরণে, আপনার এই হবে: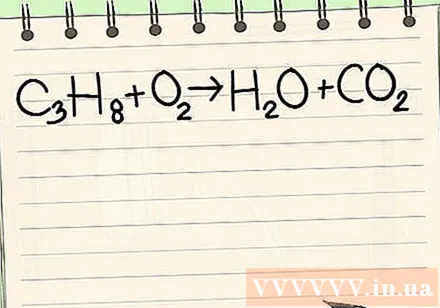
- গ3এইচ8 + ও2 -> এইচ2O + CO2
- এই বিক্রিয়া ঘটে যখন প্রোপেন (সি3এইচ8জল এবং কার্বন ডাই অক্সাইড গঠনে অক্সিজেনে পুড়ে গেছে।

সমীকরণের প্রতিটি পাশে আপনার প্রতিটি উপাদানের জন্য পরমাণুর সংখ্যা লিখুন। সমীকরণে পরমাণুর সংখ্যা জানতে প্রতিটি পরমাণুর নীচের সূচীগুলি দেখুন।- বাম: 3 কার্বন, 8 হাইড্রোজেন এবং 2 অক্সিজেন।
- ডান: 1 কার্বন, 2 হাইড্রোজেন এবং 3 অক্সিজেন।
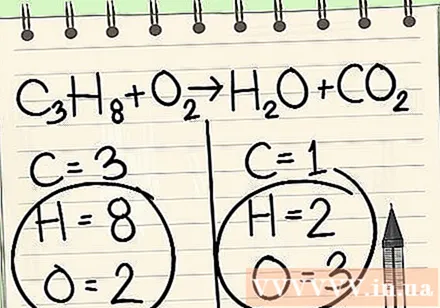
সবসময় শেষ পর্যন্ত হাইড্রোজেন এবং অক্সিজেন ছেড়ে দিন।
আপনার যদি ভারসাম্য রক্ষার জন্য একাধিক উপাদান অবশিষ্ট থাকে: এমন একটি উপাদান নির্বাচন করুন যা কেবল বিক্রিয়কের একক অণুতে এবং কেবলমাত্র পণ্যের একক অণুতে উপস্থিত হয়। এর অর্থ হ'ল আপনাকে প্রথমে কার্বন পরমাণুর ভারসাম্য বজায় রাখতে হবে।
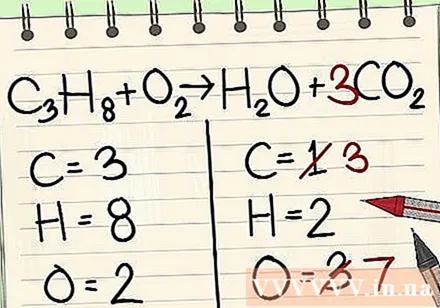
সমীকরণের বাম পাশের তিনটি কার্বন পরমাণুর সাথে ভারসাম্য বজায় রাখার জন্য সমীকরণের ডানদিকে একক কার্বন পরমাণুর জন্য সহগ যোগ করুন।- গ3এইচ8 + ও2 -> এইচ2O + 3CO2
- ডানদিকে কার্বনের সামনে 3 টির একটি ফ্যাক্টর ইঙ্গিত দেয় যে 3 টি কার্বন পরমাণু রয়েছে বামদিকে উপ -3 হিসাবে 3 কার্বন পরমাণু নির্দেশ করে।
- রাসায়নিক সমীকরণে, আপনি সহগ পরিবর্তন করতে পারেন, তবে সাবস্ক্রিপ্টটি নয়।
এরপরে হাইড্রোজেন পারমাণবিক ভারসাম্য। আপনার বাম দিকে 8 টি হাইড্রোজেন পরমাণু রয়েছে। সুতরাং আপনার ডান পাশে 8 টি লাগবে।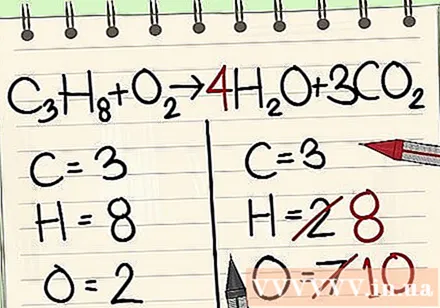
- গ3এইচ8 + ও2 -> 4 এইচ2O + 3CO2
- ঘন্টাটির ডানদিকে আপনি 4 টি যোগ করুন কারণটি নীচের সংখ্যাটি দেখায় যে আপনার কাছে ইতিমধ্যে 2 টি হাইড্রোজেন পরমাণু রয়েছে।
- আপনি যখন সূচক 2 দ্বারা গুণনক 4 গুন করেন, আপনি 8 পাবেন।
- অন্যান্য 6 অক্সিজেন পরমাণু 3CO থেকে are2(3x2 = 6 অক্সিজেন পরমাণু + 4 অন্যান্য অক্সিজেন পরমাণু = 10)
ভারসাম্য অক্সিজেন পরমাণু।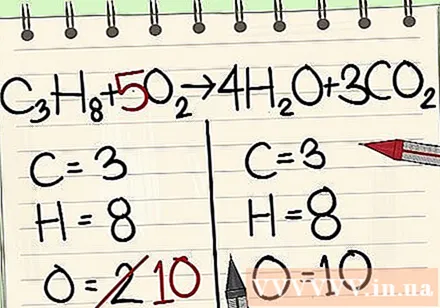
- আপনি সমীকরণের ডানদিকে অণুগুলিতে সহগ যোগ করেছেন বলে অক্সিজেন পরমাণুর সংখ্যা পরিবর্তিত হয়েছে has এখন আপনার কাছে পানির অণুতে 4 টি অক্সিজেন পরমাণু এবং কার্বন ডাই অক্সাইড অণুতে 6 অক্সিজেন পরমাণু রয়েছে। মোট আমাদের 10 টি অক্সিজেন পরমাণু রয়েছে।
- সমীকরণের বামে অক্সিজেন অণুতে 5 গুণকটি যুক্ত করুন। এখন আপনার প্রতিটি দিকে 10 টি অক্সিজেন অণু রয়েছে।
- গ3এইচ8 + 5O2 -> 4 এইচ2O + 3CO2.

- কার্বন, হাইড্রোজেন এবং অক্সিজেন পরমাণু ভারসাম্যহীন। আপনার সমীকরণ সম্পূর্ণ।
পদ্ধতি 2 এর 2: বীজগণিত পদ্ধতি অনুসারে ভারসাম্য
প্রতীক এবং সূত্র অনুযায়ী সমীকরণ লিখুন। উদাহরণস্বরূপ a = 1 এবং সেই সূত্রের ভিত্তিতে সমীকরণটি লিখুন।
অঙ্কগুলি তাদের ভেরিয়েবলের সাথে প্রতিস্থাপন করুন।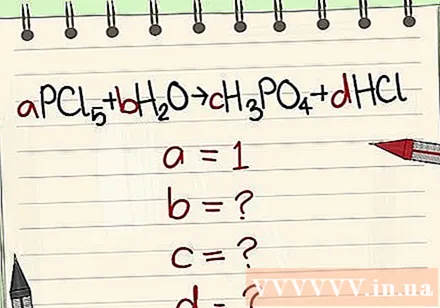
প্রতিক্রিয়া পক্ষের পাশাপাশি পণ্যের অংশের পরিমাণের পরিমাণ পরীক্ষা করে দেখুন।
- উদাহরণ: aPCl5 + bH2O = cH3PO4 + dHCl যাতে একটি = 1 বি = সি = ডি = এবং পি, সিএল, এইচ, হে উপাদানগুলি পৃথক করে, যাতে আপনি একটি = 1 বি = 4 সি = 1 ডি = 5 পান ।
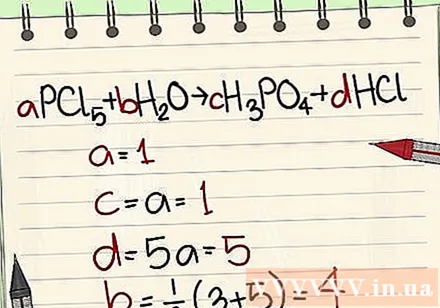
- উদাহরণ: aPCl5 + bH2O = cH3PO4 + dHCl যাতে একটি = 1 বি = সি = ডি = এবং পি, সিএল, এইচ, হে উপাদানগুলি পৃথক করে, যাতে আপনি একটি = 1 বি = 4 সি = 1 ডি = 5 পান ।
পরামর্শ
- সমীকরণটি সহজ করার জন্য মনে রাখবেন।
- আপনার যদি সমস্যা হয় তবে এটি ভারসাম্য বজায় রাখতে আপনি অনলাইন ভারসাম্য সরঞ্জামে কোনও সমীকরণ টাইপ করতে পারেন। মনে রাখবেন আপনি যখন পরীক্ষা দেন তখন আপনার কোনও অনলাইন ব্যালেন্স অ্যাক্সেস থাকে না, তাই এটির উপর নির্ভর করবেন না।
সতর্কতা
- রাসায়নিক সমীকরণে ভগ্নাংশ হিসাবে কোনও গুণাগুণ কখনই ব্যবহার করবেন না - আপনি রাসায়নিক বিক্রিয়ায় অণু বা পরমাণুকে ভাগ করতে পারবেন না।
- ভারসাম্য প্রক্রিয়া চলাকালীন আপনি ভগ্নাংশ ব্যবহার করতে পারেন তবে সহগগুলি এখনও ভগ্নাংশ থাকলে সমীকরণটি ভারসাম্যপূর্ণ হবে না।
- ভগ্নাংশ অপসারণ করতে ভগ্নাংশের ডিনোমিনেটর দ্বারা সম্পূর্ণ সমীকরণ (বাম এবং ডান উভয়) গুণফল করুন।