লেখক:
Helen Garcia
সৃষ্টির তারিখ:
21 এপ্রিল 2021
আপডেটের তারিখ:
1 জুলাই 2024

কন্টেন্ট
একটি রাসায়নিক সমীকরণ একটি রাসায়নিক বিক্রিয়ের প্রতীকী উপস্থাপনা। এই ক্ষেত্রে, প্রতিক্রিয়াশীল যৌগগুলি (রিএজেন্টস) বাম দিকে লেখা হয়, এবং ফলে পদার্থ (প্রতিক্রিয়া পণ্য) - সমীকরণের ডান দিকে। তাদের মধ্যে বাম থেকে ডানে একটি তীর স্থাপন করা হয়েছে, যা প্রতিক্রিয়ার দিক নির্দেশ করে। ভর সংরক্ষণের আইন অনুসারে, রাসায়নিক বিক্রিয়া চলাকালীন, নতুন পরমাণু উপস্থিত হতে পারে না বা পুরাতনগুলি অদৃশ্য হয়ে যায় না; অতএব, বিক্রিয়কগুলিতে পরমাণুর সংখ্যা রাসায়নিক বিক্রিয়া পণ্যগুলিতে পরমাণুর সংখ্যার সমান হতে হবে । এই নিবন্ধে বর্ণনা করা হয়েছে কিভাবে বিভিন্ন পদ্ধতি ব্যবহার করে রাসায়নিক সমীকরণের ভারসাম্য বজায় রাখা যায়।
ধাপ
2 এর পদ্ধতি 1: গতানুগতিক পদ্ধতি
 1 একটি রাসায়নিক সমীকরণ লিখ। একটি উদাহরণ হিসাবে, নিম্নলিখিত প্রতিক্রিয়া বিবেচনা করুন:
1 একটি রাসায়নিক সমীকরণ লিখ। একটি উদাহরণ হিসাবে, নিম্নলিখিত প্রতিক্রিয়া বিবেচনা করুন: - গ3জ8 + ও2 -> এইচ2ও + সিও2
- এই প্রতিক্রিয়া প্রোপেনের দহন বর্ণনা করে (সি3জ8) জল এবং কার্বন ডাই অক্সাইড (কার্বন ডাই অক্সাইড) গঠনে অক্সিজেনের উপস্থিতিতে।
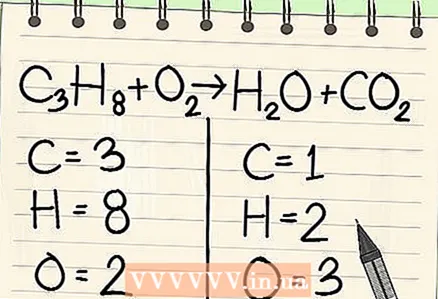 2 প্রতিটি মৌলের পরমাণুর সংখ্যা লিখ। সমীকরণের উভয় পক্ষের জন্য এটি করুন। পরমাণুর মোট সংখ্যা নির্ধারণ করতে প্রতিটি উপাদানের পাশে সাবস্ক্রিপশনগুলি লক্ষ্য করুন। সমীকরণে প্রতিটি উপাদানের প্রতীক লিখ এবং পরমাণুর সংশ্লিষ্ট সংখ্যা নোট কর।
2 প্রতিটি মৌলের পরমাণুর সংখ্যা লিখ। সমীকরণের উভয় পক্ষের জন্য এটি করুন। পরমাণুর মোট সংখ্যা নির্ধারণ করতে প্রতিটি উপাদানের পাশে সাবস্ক্রিপশনগুলি লক্ষ্য করুন। সমীকরণে প্রতিটি উপাদানের প্রতীক লিখ এবং পরমাণুর সংশ্লিষ্ট সংখ্যা নোট কর। - উদাহরণস্বরূপ, বিবেচনাধীন সমীকরণের ডান দিকে, সংযোজনের ফলে, আমরা 3 টি অক্সিজেন পরমাণু পাই।
- বাম দিকে, আমাদের 3 টি কার্বন পরমাণু আছে (C3), 8 হাইড্রোজেন পরমাণু (এইচ8) এবং 2 অক্সিজেন পরমাণু (ও2).
- ডান দিকে আমাদের 1 টি কার্বন পরমাণু (সি), 2 টি হাইড্রোজেন পরমাণু (এইচ2) এবং 3 অক্সিজেন পরমাণু (O + O2).
 3 পরে হাইড্রোজেন এবং অক্সিজেন সংরক্ষণ করুন, কারণ তারা বাম এবং ডান দিকে বেশ কয়েকটি যৌগের অংশ। হাইড্রোজেন এবং অক্সিজেন বেশ কয়েকটি অণুর অংশ, তাই তাদের মধ্যে সর্বশেষ ভারসাম্য রাখা ভাল।
3 পরে হাইড্রোজেন এবং অক্সিজেন সংরক্ষণ করুন, কারণ তারা বাম এবং ডান দিকে বেশ কয়েকটি যৌগের অংশ। হাইড্রোজেন এবং অক্সিজেন বেশ কয়েকটি অণুর অংশ, তাই তাদের মধ্যে সর্বশেষ ভারসাম্য রাখা ভাল। - হাইড্রোজেন এবং অক্সিজেনের ভারসাম্য বজায় রাখার আগে, আপনাকে পরমাণুগুলি আবার গণনা করতে হবে, কারণ অন্যান্য উপাদানগুলির ভারসাম্য বজায় রাখার জন্য অতিরিক্ত কারণগুলির প্রয়োজন হতে পারে।
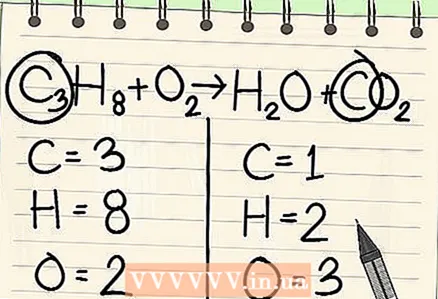 4 সর্বনিম্ন ঘন ঘন আইটেম দিয়ে শুরু করুন। যদি আপনার বেশ কয়েকটি উপাদানের ভারসাম্য বজায় রাখার প্রয়োজন হয়, তবে এমন একটি চয়ন করুন যা একটি রিএজেন্ট অণুর অংশ এবং প্রতিক্রিয়া পণ্যগুলির একটি অণু। সুতরাং, কার্বন আগে সুষম হতে হবে।
4 সর্বনিম্ন ঘন ঘন আইটেম দিয়ে শুরু করুন। যদি আপনার বেশ কয়েকটি উপাদানের ভারসাম্য বজায় রাখার প্রয়োজন হয়, তবে এমন একটি চয়ন করুন যা একটি রিএজেন্ট অণুর অংশ এবং প্রতিক্রিয়া পণ্যগুলির একটি অণু। সুতরাং, কার্বন আগে সুষম হতে হবে। 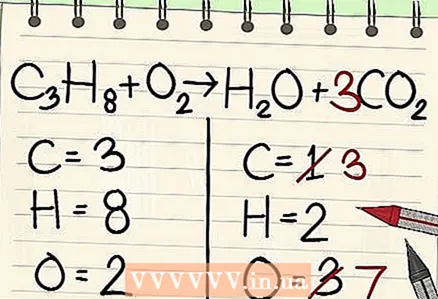 5 ভারসাম্যের জন্য, একটি একক কার্বন পরমাণুর সামনে একটি ফ্যাক্টর যোগ করুন। সমীকরণের ডান পাশে একক কার্বনের সামনে একটি ফ্যাক্টর রাখুন বাম দিকে 3 কার্বন দিয়ে এটি ভারসাম্য বজায় রাখুন।
5 ভারসাম্যের জন্য, একটি একক কার্বন পরমাণুর সামনে একটি ফ্যাক্টর যোগ করুন। সমীকরণের ডান পাশে একক কার্বনের সামনে একটি ফ্যাক্টর রাখুন বাম দিকে 3 কার্বন দিয়ে এটি ভারসাম্য বজায় রাখুন। - গ3জ8 + ও2 -> এইচ2O + 3CO2
- সমীকরণের ডান দিকে কার্বনের সামনে 3 এর একটি ফ্যাক্টর নির্দেশ করে যে তিনটি কার্বন পরমাণু রয়েছে, যা বাম পাশে প্রোপেন অণুর তিনটি কার্বন পরমাণুর সাথে মিলে যায়।
- একটি রাসায়নিক সমীকরণে, আপনি পরমাণু এবং অণুর সামনে সহগ পরিবর্তন করতে পারেন, কিন্তু সাবস্ক্রিপশনগুলি অপরিবর্তিত থাকতে হবে।
 6 তারপর হাইড্রোজেন পরমাণুর ভারসাম্য বজায় রাখুন। আপনি বাম এবং ডান দিকে কার্বন পরমাণুর সংখ্যা সমান করার পরে, হাইড্রোজেন এবং অক্সিজেন ভারসাম্যহীন রয়ে গেল। সমীকরণের বাম দিকে 8 টি হাইড্রোজেন পরমাণু রয়েছে, একই সংখ্যাটি ডানদিকে থাকা উচিত। অনুপাত দিয়ে এটি অর্জন করুন।
6 তারপর হাইড্রোজেন পরমাণুর ভারসাম্য বজায় রাখুন। আপনি বাম এবং ডান দিকে কার্বন পরমাণুর সংখ্যা সমান করার পরে, হাইড্রোজেন এবং অক্সিজেন ভারসাম্যহীন রয়ে গেল। সমীকরণের বাম দিকে 8 টি হাইড্রোজেন পরমাণু রয়েছে, একই সংখ্যাটি ডানদিকে থাকা উচিত। অনুপাত দিয়ে এটি অর্জন করুন। - গ3জ8 + ও2 -> 4 এইচ2O + 3CO2
- আমরা ডানদিকে 4 এর একটি ফ্যাক্টর যুক্ত করেছি, যেহেতু সাবস্ক্রিপ্ট দেখায় যে আমাদের ইতিমধ্যে দুটি হাইড্রোজেন পরমাণু রয়েছে।
- যদি আপনি সাবস্ক্রিপ্ট 2 দ্বারা ফ্যাক্টর 4 কে গুণ করেন, তাহলে আপনি 8 পাবেন।
- ফলস্বরূপ, ডান দিকে 10 টি অক্সিজেন পরমাণু পাওয়া যায়: 3x2 = 6 পরমাণু তিনটি 3CO অণুতে2 এবং চারটি জলের অণুতে আরও চারটি পরমাণু।
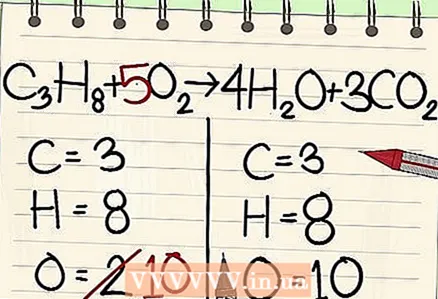 7 অক্সিজেন পরমাণুর ভারসাম্য বজায় রাখুন। অন্যান্য পরমাণুর ভারসাম্য বজায় রাখতে যে সহগ ব্যবহার করেছিলেন তা মনে রাখবেন। কারণ আপনি সমীকরণের ডান পাশে অণুর সামনে সহগ যোগ করেছেন, অক্সিজেন পরমাণুর সংখ্যা পরিবর্তিত হয়েছে। আপনার এখন জলের অণুতে 4 টি অক্সিজেন পরমাণু এবং কার্বন ডাই অক্সাইড অণুতে 6 টি অক্সিজেন পরমাণু রয়েছে। সুতরাং, ডান দিকে 10 টি অক্সিজেন পরমাণু রয়েছে।
7 অক্সিজেন পরমাণুর ভারসাম্য বজায় রাখুন। অন্যান্য পরমাণুর ভারসাম্য বজায় রাখতে যে সহগ ব্যবহার করেছিলেন তা মনে রাখবেন। কারণ আপনি সমীকরণের ডান পাশে অণুর সামনে সহগ যোগ করেছেন, অক্সিজেন পরমাণুর সংখ্যা পরিবর্তিত হয়েছে। আপনার এখন জলের অণুতে 4 টি অক্সিজেন পরমাণু এবং কার্বন ডাই অক্সাইড অণুতে 6 টি অক্সিজেন পরমাণু রয়েছে। সুতরাং, ডান দিকে 10 টি অক্সিজেন পরমাণু রয়েছে। - সমীকরণের বাম পাশে অক্সিজেন অণুতে 5 এর একটি গুণক যুক্ত করুন। প্রতিটি টুকরোতে এখন 10 টি অক্সিজেন পরমাণু রয়েছে।
- গ3জ8 + 5O2 -> 4 এইচ2O + 3CO2.

- সুতরাং, সমীকরণের উভয় পাশে একই সংখ্যক কার্বন, হাইড্রোজেন এবং অক্সিজেন পরমাণু রয়েছে। সমীকরণটি ভারসাম্যপূর্ণ।
2 এর পদ্ধতি 2: বীজগণিত পদ্ধতি
- 1 বিক্রিয়া সমীকরণ লিখ। উদাহরণস্বরূপ, নিম্নলিখিত রাসায়নিক প্রতিক্রিয়া বিবেচনা করুন:
- পিসিএল5 + এইচ2ও -> এইচ3PO4 + HCl
- 2 প্রতিটি সংযোগের সামনে একটি চিঠি রাখুন:
- কপিসিএল5 + খজ2ও -> গজ3PO4 + ঘHCl
- 3 সমীকরণের বাম এবং ডান দিকে প্রতিটি উপাদানের পরমাণুর সংখ্যা সমান করুন।
- কপিসিএল5 + খজ2ও -> গজ3PO4 + ঘHCl
- বাম দিকে আমাদের 2 টি আছেখ হাইড্রোজেন পরমাণু (প্রতিটি H তে 22O), যখন ডানদিকে 3গ+ঘ হাইড্রোজেন পরমাণু (প্রতি H তে 33PO4 এবং প্রতিটি HCl অণুতে 1)। যেহেতু বাম এবং ডান দিকে একই হাইড্রোজেন পরমাণু থাকতে হবে, 2খ 3 এর সমান হওয়া উচিতগ+ঘ.
- সমস্ত উপাদানগুলির জন্য এটি করুন:
- পি: ক=গ
- Cl: 5ক=ঘ
- H: 2খ=3গ+ঘ
- 4 সহগের সংখ্যাসূচক মান বের করার জন্য সমীকরণ পদ্ধতির সমাধান করুন। সিস্টেমের বেশ কয়েকটি সমাধান আছে, যেহেতু সমীকরণের চেয়ে বেশি ভেরিয়েবল রয়েছে। এমন একটি সমাধান খুঁজে বের করা প্রয়োজন যাতে সমস্ত সহগের ক্ষুদ্রতম সম্ভাব্য পূর্ণসংখ্যার আকার থাকে।
- সমীকরণের একটি সিস্টেম দ্রুত সমাধান করতে, ভেরিয়েবলের একটিতে একটি সংখ্যাসূচক মান নির্ধারণ করুন। ধরুন a = 1। আসুন সিস্টেমটি সমাধান করি এবং অবশিষ্ট ভেরিয়েবলের মানগুলি খুঁজে বের করি:
- P a = c এর জন্য c = 1
- Cl 5a = d এর জন্য d = 5
- যেহেতু H 2b = 3c + d এর জন্য, আমরা b মানটি খুঁজে পাই:
- 2b = 3 (1) + 5
- 2b = 3 + 5
- 2b = 8
- b = 4
- সুতরাং, আমাদের নিম্নলিখিত সহগ আছে:
- a = 1
- b = 4
- c = 1
- d = 5
পরামর্শ
- যদি আপনার অসুবিধা হয়, রাসায়নিক সমীকরণের ভারসাম্য বজায় রাখতে একটি অনলাইন ক্যালকুলেটর ব্যবহার করা যেতে পারে। তবে দয়া করে মনে রাখবেন, পরীক্ষার সময় এই ধরনের ক্যালকুলেটর ব্যবহার করার অনুমতি নেই, তাই শুধুমাত্র এর উপর নির্ভর করবেন না।
- মনে রাখবেন, কখনও কখনও সমীকরণটি সরল করা যায়! যদি সমস্ত সহগ এমনকি একটি পূর্ণসংখ্যা দ্বারা বিভাজ্য হয়, সমীকরণটি সরল করুন।
সতর্কবাণী
- ভগ্নাংশের সহগ থেকে পরিত্রাণ পেতে, ভগ্নাংশের হর দ্বারা পুরো সমীকরণ (এর বাম এবং ডান দিক) গুণ করুন।
- রাসায়নিক সমীকরণের সহগ হিসাবে কখনো ভগ্নাংশ ব্যবহার করবেন না - রাসায়নিক বিক্রিয়ায় অর্ধেক অণু বা পরমাণু নেই।
- ভারসাম্য প্রক্রিয়ায়, আপনি সুবিধার জন্য ভগ্নাংশ ব্যবহার করতে পারেন, কিন্তু সমীকরণটি ততক্ষণ ভারসাম্যপূর্ণ নয় যতক্ষণ না এতে ভগ্নাংশের সহগ আছে।